Депрессия. Нейтральные жиры, масла: общая характеристика, окисление, гидрогенизация
К нейтральным жирам относится группа липидов, состоящих из трехатом-ного спирта — глицерина и трех остатков жирных кислот, поэтому они на-зываются триглицеридами.
В состав нейтральных жиров могут входить одинаковые жирные кислоты, например пальмитиновая . В таком случае образуется сложный эфир - триглицерид, трипальмитин. Это простые жиры. Если жиры содержат остатки разных жирных кислот, то образуются смешанные жиры.
В данном уравнении реакции показаны обратимые процессы синтеза (верхняя стрелка) и гидролиза (нижняя) жира.
Природные жиры отличаются большим разнообразием входящих в их состав жирных кислот, их различным расположением в молекуле и степенью ненасыщенности. Потенциально могут существовать миллионы изомеров триглицеридов.
Жирные кислоты — органические кислоты с длинной углеводородной цепью (радикалом R), содержащей от 4 до 24 и более атомов углерода , и одной карбоксильной группой. Общая формула жирных кислот имеет вид
СnН2n + 1СООН, или R-COOH.
Для многих жирных кислот характерно наличие четного числа атомов углерода, что обусловлено, по-видимому, их синтезом путем прибавления двууглеродных звеньев к растущей углеводородной цепи.
В состав жиров организма человека чаще всего входят жирные кислоты с 16 или 18 атомами углерода, которые называются высшими жирны-ми кислотами. Высшие жирные кислоты разделяются на насыщенные предельные) и ненасыщенные (непредельные)
В насыщенных жирных кислотах все свободные связи углеродных атомов заполнены водородом. Такие жирные кислоты не имеют двойных или тройных связей в углеродной цепи. Ненасыщенные жирные кислоты имеют в углеродной цепи двойные связи (-С=С-), первая из которых возникает между девятым и десятым атомами углерода от карбоксильной группы. Жирные кислоты с тройными связями встречаются редко. Жирные кислоты, содержащие две и более двойных связей, называются полинена-сыщенными.
С увеличением числа углеродных атомов в молекулах жирных кислот температура их плавления увеличивается. Жирные кислоты могут быть твердыми веществами (например, стеариновая) либо жидкими (например, линолевая, арахидоновая); они не растворимы в воде и весьма слабо рас-творимы в спирте.
Твердые жиры — это жиры животного происхождения, за исключением рыбьего жира. Жидкие жиры — это растительные масла, за исключением кокосового и пальмового масел, которые затвердевают при охлаждении. В организме животных и у растений ненасыщенных жирных кислот в два раза больше, чем насыщенных.
Ненасыщенные жирные кислоты более реакционноспособны, чем на-сыщенные. Они легко присоединяют два атома водорода по месту двойных связей, превращаясь в насыщенные:
Этот процесс называется гидрогенизацией. Вещества, подвергнутые гидрогенизации, изменяют свои свойства. Например, растительные масла превращаются в твердый жир. Реакция гидрогенизации широко использу-ется для получения твердого пищевого жира — маргарина из жидких рас-тительных масел.
Особое значение для человека имеют полиненасыщенные жирные кислоты. В организме они не синтезируются. При их недостатке или отсутствии в пи-ще нарушается обмен жиров, в частности холестерина, наблюдаются па-тологические изменения в печени, коже, функции тромбоцитов. Поэтому такие ненасыщенные жирные кислоты, как линоленовая и линолевая, — незаменимые факторы питания.
Кроме того, они способствуют выходу из печени жиров, которые синтезируются в ней, и предупреждают ее ожи-рение. Такое действие ненасыщенных жирных кислот называется липотропным эффектом. Ненасыщенные жирные кислоты служат предшествен-никами синтеза биологически активных веществ — простагландинов. Су-точная потребность человека в полиненасыщенных кислотах в норме сос-тавляет примерно 15 г.
Нейтральные жиры накапливаются в жировых клетках (адипоцитах), под кожей, в молочных железах, жировых капсулах вокруг внутренних органов брюшной полости; незначительное их количество находится в скелетных мышцах. Образование и накопление нейтральных жиров в жировых тканях называется депонированием. Триглицериды составляют основу резервных жиров, которые являются энергетическим запасом организма и используются при голодании, недостаточном употреблении жиров, длительных физических нагрузках.
Нейтральные жиры входят также в состав клеточных мембран, сложных белков протоплазмы и называются протоплазматическими. Протоплазматические жиры не используются в качестве энергетического источника даже при истощении организма, так как выполняют структурную функцию. Их количество и химический состав постоянны и не зависят от состава пищи, тогда как состав резервных жиров постоянно изменяется. У человека протоплазматические жиры составляют около 25 % всей массы жира в организме (2-3 кг).
В различных клетках организма, особенно в жировой ткани, постоянно протекают ферментативные реакции биосинтеза и распада нейтральных жиров:
При гидролизе жиров в организме образуются глицерин и свобод-ные жирные кислоты. Этот процесс катализируется ферментами липаза-ми. Процесс гидролиза жиров в тканях организма называется липолизом. Скорость липолиза значительно увеличивается при физических нагрузках на выносливость, а активность липаз повышается в процессе тренировки.
Если реакцию распада жира проводить в присутствии щелочей (NaOH, КОН), то образуются натриевые или калиевые соли жирных кислот, кото-рые называются мылами, а сама реакция — омылением. Эта химическая реакция лежит в основе производства мыла из различ-ных жиров и их смесей.
Фосфолипиды
Фосфолипиды — это жироподобные вещества, состоящие из спирта (чаще глицерина), двух остатков жирных кислот, остатка фосфорной кислоты и азотсодержащего вещества (аминоспирта — холина или коламина).
Если в молекулы фосфолипида входит холин, они называются лецитины, а если коламин - кефалины.
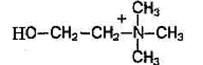
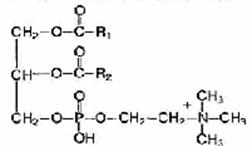
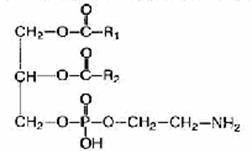 Холин Коламин
Холин Коламин
Альфа-лецитин Альфа-кефалин
Строение бета-изомеров отличается тем, что остатки фосфорной кислоты и аминоспирта расположены у второго (среднего) углеродного атома глицерина.
Фосфатиды , особенно лецитин в большом количестве содержатся в желтке яиц. В организме человека они широко распространены в нервной ткани. Фосфолипиды играют важную биологическую роль, являясь структур-ным компонентом всех клеточных мембран, поставщиками холина, необ-ходимого для образования нейропередатчика — ацетилхолина. От фосфолипидов зависят такие свойства мембран, как проницаемость, рецепторная функция, каталитическая активность мембраносвязанных ферментов.
Фосфолипиды доминируют в мембранах животной клетки, они содержатся также во многих ее субклеточных частицах.
Биологическая роль фосфолипидов в организме значительна и разнообразна. В качестве непременного компонента биологических мембран фофолипиды принимают участие в их барьерной, транс-портной, рецепторной функциях, в разделении внутреннего прост-ранства клетки на клеточные органеллы — «цистерны», отсеки. Эти функции мембран относят в настоящее время к важнейшим регуляторным механизмам жизнедеятельности клеток. Присутствие фосфолипидов в мембранах необходимо и для функционирования мембранносвязанных ферментных систем.
СТЕРОИДЫ

Стероиды относятся к неомыляемым липидам. По химической природе стероиды - производные циклопентанпергидрофенантрена. Их разделяют на стерины и стериды. Стерины — высокомолеку-лярные циклические спирты, имеющие в составе молекулы ядро циклопентанпергидрофенантрена.
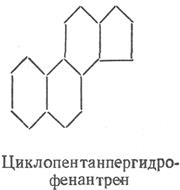 |
В состав различных тканей входят также стериды — сложные эфиры, образованные стеринами и жирными кислотами. Стерины и их производные выполняют разнообразные функции в орга-низме. Большое биологическое значение в животном организме имеет холестерин . Нарушение его обмена может повлечь патологические изменения сосудов — атеросклероз. Холестерин служит биологиче-ским предшественником желчных кислот, стероидных гормонов. Желчные кислоты имеют большое значение в процессе расщепле-ния липидов в кишечнике. Стероидные гормоны регулируют мно-гочисленные процессы обмена веществ.
БЕЛКИ
Наиболее важными соединениями каждого организма являются белки. Они обязательно обнаруживаются во всех клетках организма, в большинстве из них на долю белка приходится более поло-вины сухого остатка. Все основные проявления жизни связаны с белками. «Жизнь, — писал Ф. Энгельс, — есть способ существования белковых тел... Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым телом, и повсюду, где мы встречаем какое-либо белковое тело, не находящееся в процессе разложения, мы без исключения встречаем и проявления жизни».
Белки - высокомолекулярные азотосодержащие органические соединения, состоящие из остатков аминокислот. В составе неко-торых белков наряду с аминокислотами обнаруживают и другие соединения.
Для живых организмов характерно большое разнообразие белков, которые составляют основу структуры организма и обеспечи-вают множество его функций. Полагают, что в природе существу-ет примерно 1010-1012 различных белков, что и объясняет большое многообразие живых организмов. В одноклеточных орга-низмах насчитывают около 3000 различных белков, а в организме человека — около 5000000.
Несмотря на сложность строения и многообразие, все белки построены из сравнительно простых структурных элементов — аминокислот. Белки представляют собой полимерные молекулы, в состав которых входит 20 различных аминокислот. Изменение числа аминокислотных остатков и последовательности их распо-ложения в молекуле белка обеспечивает возможность образова-ния громадного количества белков, отличающихся своими физико-химическими свойствами, структурной или функциональной ролью в организме.
Для любого организма белки играют решающую роль во всех процессах жизнедеятельности. С ними связа-ны такие свойства живого организма, как раздражи-мость, сократимость, пищеварение, способность к росту, размножению, движению. Следовательно, бел-ки являются главными носителями жизни. В неживой природе соединения, подобные белкам, не встреча-ются.
Химический состав и биологическая роль белков
Белки — высокомолекулярные азотсодержащие ве-щества, при гидролизе которых образуются амино-кислоты. Иногда белки называют протеинами (от греч. proteus — первый, главный), определяя тем са-мым их важнейшую роль в жизнедеятельности всех организмов. Белок в организме человека составляет в среднем 45 % сухой массы тела (12-14 кг). Содержа-ние его в отдельных тканях различное. Наибольшее количество белка содержится в мышцах, костях, коже, пищеварительном тракте и других плот-ных тканях.
Суточная потребность в белке взрослого челове-ка, не занимающегося спортом, составляет в среднем 1,3 г на 1 кг массы тела или около 80 г. При больших энерготратах потребность в них увеличивается при-мерно на 10 г на каждые 2100 кДж увеличивающихся затрат энергии.
Белки поступают в организм преимущественно с пищей животного происхождения. В растениях бел-ков содержится значительно меньше: в овощах и фруктах — всего 0,3-2,0 % массы свежей ткани; наи-большее количество белков — в бобовых — 20-30 %, злаках — 10-13 и грибах — 3-6 %.
Элементарный состав белков . Важнейшими хи-мическими элементами всех белков являются углерод (50-55 %), кислород (21-23 %), водород (6,5-7,3%), азот (15-18%), сера (0,3-2,5%). В составе белков обнаружены также фосфор, железо, йод, медь, марганец и другие химические элементы.
БИОХИМИЯ ЛИПИДОВ
Общая характеристика липидов
Липидами (от греч. lipos - жир) называют жиры и жироподобные вещества. Содержатся они во всех живых клетках и выполняют ряд жизненно важных функций: структурную, метаболическую, энергетическую, защитную и др. Не растворяются или слабо растворяются в воде, хорошо растворяются в органических растворителях. Большинство из них являются производными спиртов, высших жирных кислот или альдегидов.
Химические свойства и биологическое значение липидов определяются наличием в их молекулах неполярных углеродных цепей и полярных групп: -COOH,-OH,-NH 2 и др. Это дает возможность им быть поверхностно-активными, участвовать в проницаемости клеточных мембран, легко растворяться в органических растворителях, быть растворителями для витаминов и других соединений.
Различают две группы липидов: простые и сложные. Молекулы простого липида образуются из остатков спиртов (глицерина, гликолей, высших или циклических) и высших жирных кислот. Это нейтральные жиры, диольные липиды, стериды и воски. Молекулы сложного липида состоят из остатков спиртов, высших жирных кислот и других веществ (азотистых оснований, H 3 PO 4 , H 2 SO 4 , углеводов и др.). К сложным липидам относятся фосфатиды, гликолипиды, сульфатиды. Часто к липидам относят моно- и диглицериды, стерины, каротины и другие близкие к ним вещества.
Нейтральные жиры. Являются смесью триглицеридов - сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами.
Высшие жирные кислоты представлены насыщенными, ненасыщенными и циклическими карбоновыми кислотами, а в ряде случаев - оксикислотами.
Насыщенные карбоновые кислоты обычно имеют четное число атомов углерода, например:

Кислоты с нечетным числом атомов углерода часто имеют разветвленную углеродную цепь, например изовалериановая:

Ненасыщенные карбоновые кислоты могут иметь от одной до четырех двойных связей, например:
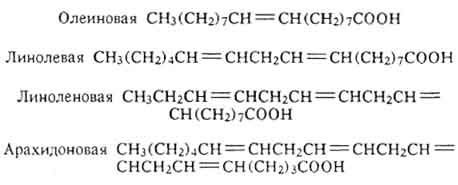
В составе жиров обнаружены остатки циклических кислот, например хаульмугровой C 17 H 29 COOH, и оксикислот, например:

Триглицериды бывают простыми и сложными. В состав молекулы простого триглицерида входят остатки одной жирной кислоты, сложного триглицерида - двух или трех жирных кислот:

Жиры широко распространены в природе. В составе жиров животного происхождения преобладают остатки
насыщенных жирных кислот, что и определяет их твердую консистенцию. Большое значение имеют коровье масло, свиное сало, бараний и говяжий жиры. Жиры растительного происхождения в своем составе преимущественно содержат остатки непредельных жирных кислот и являются жидкостями (кроме пальмитинового масла). Наиболее часто используются подсолнечное, оливковое, льняное, миндальное масло и др.
В различных продуктах и кормах содержится неодинаковое количество жиров. В растениях они сконцентрированы обычно в семенах, меньше - в плодах. Так, в семенах клещевины содержится 58-78% жира, рапса - 36-40, льна - 28,9-49, подсолнечника - 29-57, зернах кукурузы - 5, овса - 3, пшеницы 1-1,8%.
В организме животных жиры концентрируются в основном в подкожной клетчатке (до 50%), сальнике, соединительнотканных капсулах почек и гениталиев, в печени и мышечной ткани. Биологические жидкости бедны жирами. Из них относительно высокий процент жира имеет молоко (коровье - 3,5%, оленье - 17,1%). Жиры являются важнейшим источником химической энергии. Так, при тканевом окислении 1 г жира образуется 9,3 ккал (1 г углеводов дает 4,3 ккал, белков -4,1 ккал). Жиры - источник эндогенной воды: при окислении 100 г жиров в тканях образуется 107,1 г воды, что очень важно для животных, обитающих в южных широтах (например, для верблюдов) или для тех, которые впадают в зимнюю спячку (например, для бурых медведей). Жиры - растворители органических веществ, особенно жирорастворимых витаминов. Принимают участие в терморегуляции, так как обладают низкой теплоемкостью, защищают организм от механических повреждений (входят в состав капсул сердца, почек, печени, глаза), обусловливают эластичность кожи.
Различают резервные (запасные) и протоплазматические (структурные) жиры. Первые из них расходуются организмом для различных потребностей, о которых говорилось выше. Вторые являются составными частями клеточных мембран, входят в состав липопротеидных комплексов.
Жиры - продукты питания человека и животных. Растительные масла могут использоваться для
приготовления олифы и лаков. Многие из них, кроме пищевых целей и откорма животных (жмыхи), можно гидрогенизировать и получать различные сорта маргарина. Жиры из печени тресковых рыб применяют как источник витаминов A и D. Технические жиры используют в различных областях народного хозяйства (в легкой, химической и других промышленностях).
Качество и чистота жиров характеризуются физическими и химическими константами (табл. 3). Физические константы: плотность, температура плавления и застывания, коэффициент рефракции (для жидких жиров); химические константы: число омыления, Рейхарда - Мейсля, йодное, кислотное и некоторые другие показатели.
Число омыления определяется количеством миллиграммов KOH, израсходованного на нейтрализацию жирных кислот, которые образуются при омылении 1 г жира.
Число Рейхарда - Мейсля характеризуется количеством 0,1 н. раствора NaOH, пошедшего на нейтрализацию летучих жирных кислот (масляной, капроновой и каприловой), образованных при гидролизе 5 г жира и отогнанных с водяным паром.
Йодное число характеризует наличие в составе жира ненасыщенных жирных кислот и определяется количеством граммов йода, способным присоединиться к 100 г жира.
Кислотное число свидетельствует о наличии в составе жира свободных жирных кислот, которые
3. Физические и химические константы некоторых жиров
| Константы | Вид жира | ||
| говяжий | бараний | свиной | |
| Плотность при 15°C, г/см 3 | 0,923-0,933 | 0,932-0,961 | 0,931-0,938 |
| Температура плавления, °C | 42-52 | 44-55 | 36-46 |
| Температура застывания, °С | 27-38 | 32-45 | 26-32 |
| Коэффициент преломления (при 40°С) | 1,4510-1,4583 | 1,4566-1,4583 | 1,4536 |
| Число омыления | 190-200 | 192-198 | 193-200 |
| Число Рейхарда-Мейсл | я | 0,3-0,9 | |
| Йодное число | 32-47 | 31-40 | 46-56 |
| Кислотное число | 0,1-0,6 | 0,1-0,2 | 0,3-0,9 |
образуются при разложении его молекул. Оно определяется числом миллиграммов KOH, пошедшего на нейтрализацию свободных жирных кислот, которые содержатся в 1 г жира.
Рассмотренные константы зависят от зоны обитания, условий питания, возраста, пола, породы животного и от других факторов. Так, С. Л. Иванов установил, что животные, обитающие в северных широтах, имеют жиры, для которых характерны более низкие температуры плавления, чем у животных того же вида, содержащихся на юге. В составе жиров первых преобладают остатки ненасыщенных жирных кислот, вторых - насыщенных.
Диольные липиды. Эти липиды открыты в тканях растений и животных советским ученым Л. Д. Бергельсоном в 1967-1973 г. Представляют собой смесь различных сложных эфиров, образованных из двухатомных спиртов (этандиола, пропандиола, бутандиола и др.) и высших жирных кислот. Общая формула
где n = 0, 1, 2, 3.
В организме выполняют те же функции, что и жиры. Изучены мало.
Стериды . Стеридами называют сложные эфиры стеринов и высших жирных кислот (чаще всего пальмитиновой). Стерины, или стеролы, - высокомолекулярные циклические спирты, производные циклопентанпергидрофенантрена. Последний можно рассматривать как продукт конденсации гидрированного фенантрена и циклопентана. Отдельные кольца в циклопентанпергидрофенантрене обозначают буквами (А, Б, В, Г), а атомы углерода колец - цифрами.

Стерины и стериды составляют неомыляемую фракцию липидов, входят в состав клеточных мембран. В
тканях печени содержание стеридов составляет около 50% общей массы всех стеринов. Различают зоо-, фито- и микостерины. Производными стеринов являются многие стероидные гормоны (половые и коры надпочечников), желчные кислоты, витамины группы D, стероидные алкалоиды, некоторые тритерпеновые антибиотики, яды кожных желез жаб, отдельные канцерогенные вещества. Стерины - кристаллические вещества, оптически активны, почти не растворяются в воде, растворяются в органических растворителях, бесцветны, способны возгоняться, вступают в химические реакции, характерные для спиртов.
Наибольший интерес представляют холестерин и его производные - хрлестериды, которые являются сложными эфирами холестерина и высших жирных кислот. Холестерин открыл в XVIII в. Конради при исследовании желчных камней. Его много в белом веществе мозга. По химической структуре холестерин - вторичный циклический спирт.
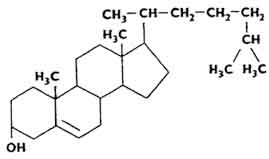
Подсчитано, что в теле человека массой 70 кг содержится около 140 г холестерина, из которого 10% сконцентрировано в надпочечниках, 2% - в нервной системе, 0,25% - в костях. Много холестерина в печени (от 0,333 до 0,91% общей массы). Холестерин способен удерживать определенное количество воды. Холестерин с белками образует комплексные соединения.
Из организма стерины выводятся главным образом в виде холестерина (см. выше) и копростерина.
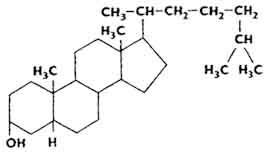
В коже животных и в неомыляемой фракции липидов находится 7-дегидрохолестерин - провитамин витамина D 3 . Дрожжи содержат эргостерин - провитамин витамина D 2 (см. главу "Витамины").
Воски. Воски - большая группа липидов, молекулы которых образованы из остатков высших жирных кислот и высших одноатомных спиртов. Соотношение углерода в кислотной и спиртовой частях молекулы равно 1:1 или 2:1. Воски содержат примеси свободных жирных кислот и спиртов, углеводородов (C 27 - С 33) и душистых веществ. По происхождению различают вески животные (пчелиный, ланолин, спермацет), растительные (карнаубский, канделильский), продукт выделения некоторых насекомых (китайский), ископаемые (церезин и монтан) и синтетические.
Пчелиный воск . Продуцируется восковыми железами пчел. Состоит из смеси сложных эфиров (до 75%), свободных высших жирных кислот и насыщенных углеводородов. Содержит витамин А и некоторые другие вещества. Основа воска - сложный эфир мирицилового спирта и пальмитиновой кислоты:
Пчелиный воск не растворяется в воде, растеряется в хлороформе и диэтиловом эфире, бензине и скипидаре. Является основой пчелиных сот. Используется для приготовления мазей и пластырей.
Ланолин . Получают после промывки шерсти овец. Представляет собой смесь сложных эфиров, образованных высшими спиртами (цетиловым, карнаубовым, холестерином и др.) и высшими жирными кислотами (ланопальмитиновой, миристиновой и др.). По физическим свойствам - это густая вязкая масса буро-желтого цвета со слабым запахом, не растворяется в воде, растворяется в хлороформе, эфире, гигроскопичен, не омыляется водными растворами щелочей, не прогоркает. Применяют для приготовления лечебных мазей и в косметике.
Спермацет . Этот компонент спермацетового масла, которое получают из головного мозга кашалотов. От одного кашалота можно получить 4-5 т
спермацета. Основная составная часть его (до 90%) -сложный эфир пальмитиновой кислоты и цетилового спирта:
Часть спермацета (10%) - сложные эфиры цетилового, стеаринового, олеинового спиртов и лауриновой, миристиновой кислот.
Спермацет - белые пластинчатые кристаллы, хорошо растворяется в диэтиловом эфире, ацетоне, горячем этаноле, не растворяется в воде. Используется для приготовления лечебных мазей и косметических средств. Применяют при лечении язв кожи.
Растительные воски . Распространены в природе. Покрывают тонким слоем листья, стебли, стволы и плоды растений. Защищают растительные ткани от травм и микробов. Участвуют в регуляции водного обмена. Представляют собой смесь сложных эфиров, образованных высшими спиртами (цетиловым, мирициловым) и жирными кислотами (церотиновой, карнаубовой, монтановой, стеариновой, пальмитиновой, олеиновой). Карнаубский воск широко используется для изготовления свеч и др. Получают его из листьев некоторых пальм. Основа воска - сложный эфир мирицилового спирта и церотиновой кислоты:
Фосфатиды . Молекула фосфатида образована остатками высших спиртов и высших жирных кислот, фосфорной кислоты и азотистого основания. С другими липидами и белками они составляют химическую основу клеточных мембран, обусловливают их избирательную проницаемость для различных веществ, участвуют в процессах клеточного дыхания и переносе электронов.
Молекула фосфатида обычно состоит из двух частей: полярной (гидрофильной) и аполярной
(гидрофобной). Гидрофильная "голова" обладает отрицательным зарядом фосфата и положительным азота, являясь перманентным диполем (цвиттер-ион). Гидрофобный "хвост" состоит из длинных цепей остатков высших жирных кислот. Именно такая структура молекулы обусловливает поверхностно-активные свойства липида, дает возможность формировать пленочные структуры в монослое на границе раздела фаз, взаимодействовать с различными (полярными и аполярными) соединениями и активно участвовать в реакциях ассимиляции и диссимиляции.
Больше всего фосфатидов содержится в нервной ткани (до 26-30% сухой массы), печени (16%), почках (11%) и сердце (10%). Они синтезируются в комплексе Гольджи.
Различают глицеро-, инозит- и сфингозинфосфатиды.
Глицерофосфатиды
Лецитины, или фолинфосфатиды . В образовании молекул α - и β -лецитинов участвуют глицерин, насыщенные и ненасыщенные высшие жирные кислоты, H 3 PO 4 и холин. В α -лецитине остаток холина и H 3 PO 4 размещаются возле атома C 1 молекулы спирта.
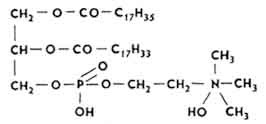
Много лецитина содержится в тканях спинного и головного мозга (35,2-12,4%), желтке куриного яйца (6,5-12%), легких, миокарде, почках (5,9-5,2%) и др. Используется организмом для биосинтеза ацетидхолина. Применяется внутрь (в виде драже) при лечении болезней нервной системы, анемиях, общем упадке сил.
Лецитином богаты также многие растительные корма: семена подсолнечника (38,5%), льна (36,2%), бобы сои (35%) и др.
Кефалины , или коламинфосфатиды . Молекулы кефалинов содержат этаноламин (коламин).
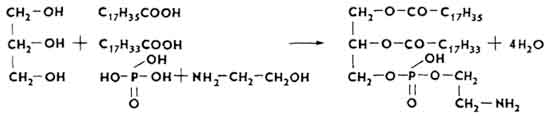
Кефалиновая фракция составляет липидную основу тканей головного мозга человека (66%), печени крупного рогатого скота (51%), миокарда (30%), желтка куриного яйца (28,7%). Богаты кефалинами бобы сои (65%), семена хлопчатника (71,2%), льна и подсолнечника (61,5%). Кефалины образуют с белками липопротеидные комплексы. Много их содержится в митохондриях.
Серинфосфатиды . В молекуле серинфосфатидов азотистым основанием является аминокислота серии.
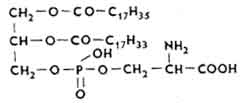
Серинфосфатидов много в нервной ткани, печени, почках и других органах. Это протошгазматические липиды. Их много в митохондриях.
Между лецитинами, кефалинами и серинфосфатидами существует генетическая связь, так как азотистые основания могут переходить друг в друга:
Ацетальфосфатиды (плазмалогены). В строении ацетальфосфатидов участвуют альдегиды высших жирных кислот. Чаще всего ацетальфосфатиды имеют следующую структуру:

Отличаются между собой азотистыми основаниями, высшими жирными килостами и их альдегидами, а также способоами образования ацеталей. Составляют около 12% всех фосфатидов тканей. Этаноламинкефалиновая фракция мозга на 2 / 3 состоит из ацетальфосфатидов; сперматозоиды на 55-60%. В отдельных органах (печень, миокард, почки, мышцы) содержание ацетальфосфатидов с возрастом увеличивается.
Кардиолипины . Впервые выделены из экстракта миокарда. Основу их молекулы составляют три остатка глицерина, соединенных между собой фосфодиэфирными связями типа 1,3 (R - остатки высших жирных кислот).

Кардиолипины занимают почти 10% всех липидов митохондрий. Эти липиды участвуют в окислительном фосфорилировании и переносе электронов, в связывании комплемента при свертывании крови.
Инозитрофосфатиды
Их молекула представляет собой сложный эфир, образованный глицерином, высшими жирными кислотами, H 3 PO 4 и шестиатомным спиртом инозитом. Различают монофосфоинозитиды и дифосфоинозитиды.
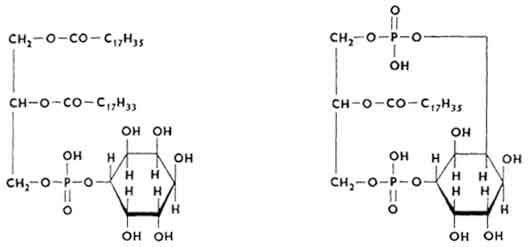
Много инозитфосфатидов выявлено в нервной ткани (мозгу), особенно в миелиновых оболочках нервных волокон. Инозитфосфатиды способны образовывать
комплексные соединения с белками. Остаток инозита может вступать в реакции с галактозой, татроновой кислотой и высшими жирными кислотами, коламином, объединяя в единое целое продукты обмена белков, углеводов и липидов, характерных для нервной ткани.
Сфингозинфосфатиды
Молекулы сфингозинфосфатидов образованы из остатков сфингозина, высших жирных кислот, фосфорной кислоты и холина.
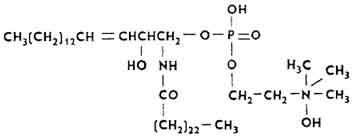
Их часто называют сфингомиелинами. Ими богаты нервная ткань (составляют основу миелиновых облочек нервных волокон), селезенка, легкие, почки, поджелудочная железа. Иногда в молекуле липида содержится остаток дигидросфингозина. Сфингозинфосфатиды - белые кристаллические вещества, образуют водный коллоидный раствор. Высшие жирные кислоты представлены стеариновой кислотой (50%), меньше - лигноцериновой и нервоновой. Составляют 20% всех липидов мозга.
Гликолипиды . Это жироподобные вещества, молекулы которых содержат также углеводный компонент.
Цереброзиды . Представляют собой смесь сложных эфиров, построенных из остатков сфингозина, высших жирных кислот и галактозы. В цереброзидах сфингозин содержится в виде цереброна - соединения с цереброновой кислотой и галактозой, керазина - соединения с лигноцериновой кислотой и галактозой и нервона - соединения с нервоновой кислотой и галактозой (см. ниже).

Цереброзидов много в тканях мозга. В составе молекулы селезенки они содержат остатки глюкозы (глюкоцереброзиды).
Цереброзиды - твердые вещества, не растворяются в воде, растворяются в диэтиловом и петролейном эфирах, при кипячении набухают, при нагревании до 200 °C разлагаются. В организме выполняют структурную и метаболическую функции.
Ганглиозиды . Молекула ганглиозида в среднем содержит 40-43% галактозы, 21% нейраминовой кислоты, 13% сфингозина, 23-26% гексозаминов, глюкозы и стеариновой кислоты. Много липидов в нервной ткани, паренхиматозных органах, клетках крови. Ганглиозиды - структурные компоненты нейронов, обезвреживают яды, участвуют в проведении нервных импульсов и т. д.
Сульфатиды . Это - сложные эфиры, образованные сфингозином, цереброновой или лигноцериновой кислотой, галактозой и серной кислотой.

Сульфатиды имеются в тканях мозга, печени, почек, мышц и др. Они появляются в моче при церебральной склерозе.
Ацилглицеролы, или нейтральные липиды, - наиболее распространенная в природе группа липидов. Эти соединения представляют собой сложные эфи-ры жирных кислот и трехатомного спирта глицерола (глицериды), в котором могут быть этерифицированы одна, две или три гидроксильные группы глицерола с образованием соответственно моно-, ди- и триацилглицеролов:
В природе наиболее часто встречаются триацилглицеролы. Поскольку все приведенные выше ацилглицеролы не содержат ионных групп, они относятся к нейтральным липидам. Если все три кислотных радикала принадлежат одной и той же жирной кислоте, то такие триацилглицеролы называют простыми, если же разным жирным кислотам, - то смешанными.
Жирные кислоты, входящие в состав триацилглицеролов, определяют их физико-химические свойства. Чем больше в липидах остатков короткоцепо-чечных и ненасыщенных кислот, тем ниже температура плавления и выше растворимость. Так, животные жиры обычно содержат значительное количество насыщенных жирных кислот, благодаря чему они при комнатной температуре остаются твердыми. Жиры, в состав которых входит много ненасыщенных кислот, будут при этих условиях жидкими; их называют маслами.
Большинство животных жиров содержат в различных соотношениях эфиры пальмитиновой, стеариновой, пальмитоолеиновой, олеиновой и линоле-новой кислот. В жире человека, плавящемся при 15 °С, содержится около 70% ненасыщенных жирных кислот, и при температуре тела он находится в жидком состоянии. Жиры из различных тканей одного организма так же, как и растительные масла, могут различаться между собой как длиной углеводородных цепей, так и степенью их ненасыщенности.
Для характеристики свойств жира используют константы, или жировые числа, - кислотное число, число омыления, йодное число.
Общим структурным фрагментом всех фосфоглицеридов является фосфатидная кислота (1,2-диацил,3-фосфоглицерол).
Фосфатидная кислота образуется в организме в процессе биосинтеза триацилгл и неролов и фосфоглицеридов как общий промежуточный метаболит; в тканях она присутствует в незначительных количествах. Следует отметить, что все природные фосфоглицериды относятся к L-ряду. Различные фосфоглицериды отличаются друг от друга дополнительными группировками, присоединенными фосфоэфирной связью к фосфатидной кислоте, т.е. R3. Состав жирных кислот различных фосфоглицеридов различается даже в пределах одного организма и наряду с замещающими группировками определяет специфичность фосфолипидов:
Фосфатидилхолин (лецитин). В своем составе содержит аминоспирт хо-лин (гидроксид 3-гидроксиэтилтриметиламмония):
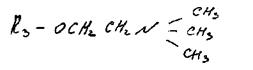 |
Фосфатидилэтаноламин (кефалин). В состав фосфатидилэтаноламинов вместо холина входит азотистое основание этаноламин НО-СН 2 -СН 2 -NH 3 .
В организме животных и в высших растениях в наибольшем количестве встречаются фосфатидилхолины и фосфатидилэтаноламины. Эти две группы глицерофосфолипидов являются главными липидными компонентами мембран клеток.
Фосфатидилинозиты В отличае от других групп фосфоглицеридов в состав фосфатидилинозитов вместо азотосодержащих соединений входит 6-углеродный циклический спирт инозитол, представленный одним из его стереоизомеров- монозитолом.
Фосфатидилглицерины. Так же как фосфатидилинозиты, фосфатидилглицерины не содержит азотсодержащего соединения. В этих соединениях полярной группой служит еще одна молекула глицерола.
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ЛИПИДОВ
Липиды - весьма разнородные по своему химическому строению вещества, характеризующиеся различной растворимостью в органических растворителях и, как правило, нерастворимые в воде. Они играют важную роль в процессах жизнедеятельности. Будучи одним из основных компонентов биологических мембран, липиды влияют на их проницаемость, участвуют в передаче нервного импульса, создании межклеточных контактов.
Другие функции липидов - образование энергетического резерва, создание защитных водоотталкивающих и термоизоляционных покровов у животных и растений, защита органов и тканей от механических воздействий. Липидная фракция содержит вещества большинство, из которых представлены в таблице. Вследствие гетерогенности входящих в липидную фракцию компонентов термин «липидная фракция» нельзя рассматривать как структурную характеристику; он является лишь рабочим лабораторным названием фракции, получаемой при экстракции биологического материала неполярными растворителями. Тем не менее, большинство липидов имеет некоторые общие структурные особенности, обусловливающие их важные биологические свойства и сходную растворимость. Наиболее распространенные липиды - это нейтральные жиры, структурным компонентом которых, как и большинства липидов, являются жирные кислоты.
НЕКОТОРЫЕ ПРИРОДНЫЕ ЖИРНЫЕ КИСЛОТЫ
|
Число атомов углерода |
Структура |
Систематическое название |
Тривиальное название |
|
Насыщенные жирные кислоты |
|||
|
СН 3 (СН 2) 10 СООН |
н- Додекановая |
Лауриновая |
|
|
СН 3 (СН 2) 12 СООН |
н- Тетрадекановая |
Миристиновая |
|
|
СН 3 (СН 2) 14 СООН |
н- Гексадекановая |
Пальмитиновая |
|
|
СН 3 (СН 2) 16 СООН |
н- Октадекановая |
Стеариновая |
|
|
СН 3 (СН 2) 18 СООН |
н- Эйкозановая |
Арахиновая |
|
|
СН 3 (СН 2) 22 СООН |
н- Тетракозановая |
Лигноцериновая |
|
|
Ненасыщенные жирные кислоты |
|||
|
СН 3 (СН 2) 5 СН =СН(СН 2) 7 СООН |
Пальмитолеиновая |
||
|
СН 3 (СН 2) 7 СН =СН(СН 2) 7 СООН |
Олеиновая |
||
|
СН 3 (СН 2) 4 СН =СНСН 2 СН=СН(СН 2) 7 СООН |
Линолевая |
||
|
СН 3 СН 2 СН =СНСН 2 СН=СНСН 2 СН=СН(СН 2) 7 СООН |
Линоленовая |
||
|
СН 3 (СН 2) 4 СН =СНСН 2 СН=СНСН 2 СН=СНСН 2 СН=(СН 2) 3 СООН |
Арахидоновая |
||
Жирные кислоты - алифатические карбоновые кислоты - в организме могут находиться в свободном состоянии (следовые количества в клетках и тканях) либо выполнять роль строительных блоков для большинства классов липидов.
Природные жирные кислоты, правда несколько условно, можно разделить на три группы: насыщенные, мононенасыщенные и полиненасыщенные жирные кислоты. Жирные кислоты, встречающиеся в природных липидах, содержат, как правило, четное число углеродных атомов и имеют по преимуществу неразветвленную цепь.
Жирные кислоты, входящие в состав липидов животных и высших растений, имеют много общих свойств. Как уже отмечалось, почти все природные жирные кислоты содержат четное число углеродных атомов, чаще всего 16 или 18. Ненасыщенные жирные кислоты животных и человека, участвующие в построении липидов, обычно содержат двойную связь между 9-м и 10-м атомами углерода; дополнительные двойные связи, как правило, бывают на участке между 10-м атомом углерода и метильным концом цепи. Своеобразие двойных связей природных ненасыщенных жирных кислот заключается в том, что они всегда отделены двумя простыми связями, т. е. между ними всегда имеется хотя бы одна метиленовая группа (-СН = СН - СН 2 - СН = СН -). Подобные двойные связи обозначают как «изолированные». Природные ненасыщенные жирные кислоты имеют цис -конфигурацию и крайне редко встречаются транс -конфигурации. Считают, что в ненасыщенных жирных кислотах с несколькими двойными связями цис -конфигурация придает углеводородной цепи изогнутый и укороченный вид, что имеет биологический смысл (особенно если учесть, что многие липиды входят в состав мембран).
Жирные кислоты с длинной углеводородной цепью практически нерастворимы в воде. Их натриевые и калиевые соли (мыла) образуют в воде мицеллы. В последних, отрицательно заряженные карбоксильные группы жирных кислот обращены к водной фазе, а неполярные углеводородные цепи спрятаны внутри мицеллярной структуры. Такие мицеллы имеют суммарный отрицательный заряд и в растворе остаются суспендированными благодаря взаимному отталкиванию.
ТЕМА. 1. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА НЕЙТРАЛЬНЫХ ЖИРОВ
(8 часов)
Нейтральные жиры - это эфиры глицерина и жирных кислот. Если жирными кислотами этерифицированы все три гидроксильные группы глицерина (ацильные радикалы R 1 ,R 2 и R 3 могут быть одинаковы или различны), то такое соединение называют триглицеридом
Глицерин (глицерол) Моноглицерид (моноацилглицерол)
(триацилглицеролом), если две - диглицеридом (диацилглице-ролом) и, наконец, если этирифицирована одна группа - моноглицеридом (моно-ацилглицеролом).
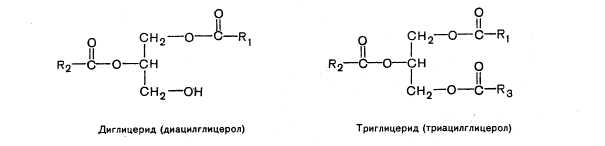
Диглицерид (диацилглицерол) Триглицерид (триацилглицерол)
Нейтральные жиры находятся в организме либо в форме протоплазматического жира, являющегося структурным компонентом клеток, либо в форме запасного, резервного жира. Роль этих двух форм жира в организме неодинакова. Протоплазматический жир имеет постоянный химический состав и содержится в тканях в определенном количестве, не изменяющемся даже при патологическом ожирении, в то время как количество резервного, жира подвергается большим колебаниям.
Основную массу природных нейтральных жиров составляют триглицериды. Жирные кислоты в триглицеридах могут быть насыщенными и ненасыщенными. Чаще среди жирных кислот встречаются пальмитиновая, стеариновая и олеиновая кислоты. Если все три кислотных радикала принадлежат одной и той же жирной кислоте, то такие триглицериды называют простыми (например, трипальмитин, тристеарин, триолеин и т. д.), если же разным жирным кислотам, - то смешанными. Названия смешанных триглицеридов образуются от входящих в их состав жирных кислот; при этом цифры 1, 2 и 3 указывают на связь остатка жирной кислоты с соответствующей спиртовой группой в молекуле глицерина (например, 1-олео-2-пальмитостеарин).
Жирные кислоты, входящие в состав триглицеридов, практически определяют их физико-химические свойства. Так, температура плавления триглицеридов повышается с увеличением числа и длинны остатков насыщенных жирных кислот. Напротив, чем выше содержание ненасыщенных жирных кислот или кислот с короткой цепью, тем ниже точка плавления. Животные жиры (сало) обычно содержат значительное количество насыщенных жирных кислот (пальмитиновой, стеариновой и др.), благодаря чему они при комнатной температуре твердые. Жиры, в состав которых входит много моно- и полиненасыщенных кислот, при обычной температуре жидкие и называются маслами. Так, в конопляном масле 95 % всех жирных кислот приходится на долю олеиновой, линолевой и линоленовой кислот и только 5 % - на долю стеариновой и пальмитиновой кислот. Заметим, что в жире человека, плавящемся при 15 °С (при температуре тела он жидкий), содержится 70% олеиновой кислоты.
Глицериды способны вступать во все химические реакции, свойственные сложным эфирам. Наибольшее значение имеет реакция омыления, в результате которой из триглицеридов образуются глицерин и жирные кислоты. Омыление жира может происходить как при ферментативном гидролизе, так и при действии кислот или щелочей.
Лабораторная работа № 40
ОБРАЗОВАНИЕ МАСЛЯНОГО ПЯТНА
Ход работы
Каплю масла наносят стеклянной палочкой на кусочек бумаги. Образуется пятно, не исчезающее при нагревании.
Лабораторная работа № 41
РАСТВОРИМОСТЬ ЖИРОВ
Реактивы : Растительное масло (подсолнечное, льняное, хлопковое или другое)
Твердый жир (бараний, говяжий)
Диэтиловый эфир, ацетон
Этиловый спирт
Ход работы
Ставят два ряда пробирок по 4 в каждом. В пробирки первого ряда вносят по нескольку капель растительного масла, в пробирки второго ряда-по кусочку твердого жира. В первую пробирку каждого ряда наливают 2 мл дистиллированной воды, во вторую - столько же диэтилового эфира, в третью - ацетона, четвертую-спирта. Все пробирки взбалтывают и наблюдают растворимость жиров в различных растворителях. Пробирки со спиртом рекомендуется подогреть на водяной бане. Записывают результаты опыта.
|
Вариант опыта |
пробирки |
Используемые реактивы (мл) |
Степень растворимости |
|||
|
Растительное масло |
||||||
Сделать вывод:
Лабораторная работа № 42
ЭМУЛЬГИРОВАНИЕ ЖИРНЫХ МАСЕЛ
Реак тивы: Растительное масло
Углекислый натрий, 2% -ный раствор
Мыло, 2%-ный раствор
Ход работы
В четыре пробирки вносят по 5 капель масла. В первую пробирку добавляют 2 мл дистиллированной воды, во вторую - 2 мл 2%-ного раствора углекислого натрия (соды), в третью - столько же 2%-ного раствора мыла, в четвертую - 2 мл воды и несколько капель желчи. Все пробирки взбалтывают и наблюдают образование в первой пробирке неустойчивой эмульсии масла в воде, быстро расслаивающейся при стоянии, а в остальных - устойчивой эмульсии благодаря действию добавленных эмульгаторов, которые адсорбируются в наружном слое жировых капель и понижают их поверхностное натяжение.
Результат опыта занести в таблицу:
|
пробирки |
Используемые реактивы (мл) |
Характер эмульсии |
||||
|
Растительное |
Н 2 О+ желчь |
|||||
|
А также студентами медицинских вузов Украины . Методические указания составлены доц . Федорко Н.Л., доц . Захариевой З.Е., доц . Вовчук... Безопасность в чрезвычайных ситуациях анализ оказания догоспитальной медицинской помощи пострадавшим в дорожно-транспортных происшествиях с сочетанными травмами в арктической зоне архангельской областиДокументВрача, студенты гуманитарных и медицинских специальностей выделили, что врач должен быть высококвалифицированным специалистом , использовать передовые методы... Л. Н. Викторова канд юр наук, доц гл. 21 (в соавт.)Документ... по проверке аптек и других медицинских учреждений , у лиц, занимающихся поделкой медицинских рецептов... может быть зафиксировано время наступления таких последствий, которое выясняется при следственном осмотре, с помощью специалиста . Указанные ... Л. С. Волкова и Заслуженный работник высшей школы рф, профессор (1)ДокументИ что по вреждение как той, так и другой производит афазию, только, может быть , форма, в которой выразится... и медицинских учреждений . В связи с тем, что студенты отделения олигофренопедагогики получают за время обучения в вузе также и логопедическую... И. А. Альтман (отв редактор), А. Е. Гербер, Ю. А. Домбровский, Ю. И. Каннер, Б. Н. Ковалев, Г. В. Костырченко, д-р Тамаш Краус (Венгрия), А. И. Круглов (Украина), Д. И. Полторак, Е. С. Розенблат (Беларусь), Л. АДокументДля специалистов системы образования – руководителей, педагогов, психологов, социальных педагогов, медицинских работников образовательных учреждений , а также ... | ||||||
Общие понятия.
Жиры - сложные эфиры глицерина и высокомолекулярных жирных кислот.
В состав жиров входят многочисленные предельные (или насыщенные) и непредельные (или ненасыщенные) жирные кислоты. Среди предельных кислот чаще встречаются стеариновая (С17Н35СООН) и пальмитиновая (С15Н31СООН). Из непредельных жирных кислот основная роль принадлежит олеиновой (С17Н33СООН), линолевой (С17Н31СООН) и линоленовой (С17Н29СООН), большое физиологическое значение имеет также арахидоновая (С19Н31СООН) кислота. Непредельные жирные кислоты характеризуются наличием двойных связей: в молекуле олеиновой кислоты содержится одна двойная связь, в молекуле линолевой - две, линоленовой - три, арахидоновой - четыре. Благодаря наличию двойных связей непредельные кислоты отличаются высокой реакционной способностью. Линолевая, линоленовая и арахидоновая (так называемые иолиненасьиценные) кислоты не синтезируются в организме человека и должны поступать с пищей. Недостаток этих кислот в пище вызывает серьезные нарушения обмена веществ, исчезающие при потреблении продуктов, в состав которых входят непредельные жирные кислоты. Поэтому указанные соединения относят к веществам, обладающим витаминным действием (витамин F). Линолевая и линоленовая кислоты содержатся в растительных маслах (льняном, подсолнечном и др.), арахидоновая кислота - в печеночных жирах рыб, сливочном масле и некоторых видах маргарина.
В состав масел некоторых тропических растений входят также циклические жирные кислоты (хаульмугро-вая, гиднокарповая и др.).
Качественные реакции на жиры.
Образование масляного пятна. Каплю масла наносят стеклянной палочкой на кусочек бумаги. Образуется пятно, не исчезающее при нагревании.
Растворимость жиров. Реактивы: а) растительное масло (подсолнечное, льняное, хлопковое или другое); б) твердый жир (бараний, говяжий); в) диэти-ловый эфир; г) ацетон; д) этиловый спирт; е) дистиллированная вода.
Ставят два ряда пробирок по 4 в каждом. В пробирки первого ряда вносят по нескольку капель растительного масла, в пробирки второго ряда- по кусочку твердого жира. В первую пробирку каждого ряда наливают 2 мл дистиллированной воды, во вторую - столько же диэтилового эфира, в третью - ацетона, четвертую - спирта. Все пробирки взбалтывают и наблюдают растворимость жиров в различных растворителях. Пробирки со спиртом рекомендуется подогреть на водяной бане. Записывают результаты опыта.
Эмульгирование жирных масел. Реактив растительное масло; б) углекислый натрий, 2%-ный раствор; в) мыло, 2%-ный раствор; г) желчь; д) дистиллированная вода.
В четыре пробирки вносят по 5 капель масла. В первую пробирку добавляют 2 мл дистиллированной воды, во вторую - 2 мл 2%-ного раствора углекислого натрия (соды), в третью - столько же 2%-ного раствора мыла, в четвертую - воды и несколько капель желчи. Все пробирки взбалтывают и наблюдают образование в первой пробирке неустойчивой эмульсии масла в воде, быстро расслаивающейся при стоянии, а в остальных - устойчивой эмульсии благодаря действию добавленных эмульгаторов, которые адсорбируются в наружном слое жировых капель и понижают их поверхностное натяжение.
Акролеиновая реакция. С помощью пробы на акролеин определяют наличие глицерина в жирах. При нагревании жира с кислым сернокислым калием натрием или борной кислотой происходит отщепление от молекулы глицерина двух молекул воды и образование акрилового альдегида, или акролеина, обладающего резким раздражающим запахом (пригоревшего сала):
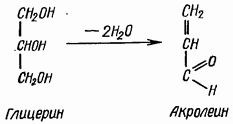
Глицерин Акролеин
Реактивы: а) растительное масло или животный жир; б) воск пчелиный; в) кислый сернокислый калий или натрий, кристаллический; г) борная кислота, кристаллическая.
В сухую пробирку вносят несколько капель растительного масла или кусочек животного жира, добавляют немного порошка кислого сернокислого калия (или натрия) или борной кислоты и осторожно подогревают. Появляются белые пары акролеина, обладающие резким запахом. Повторяют реакцию с воском - акролеин не образуется, так как глицерин не входит в состав восков.
Омыление жира. При взаимодействии жиров со щелочами происходит их гидролиз с образованием солей высших жирных кислот (мыла) и глицерина. Натриевые соли представляют собой твердые мыла, калийные - жидкие. Реакция идет по уравнению
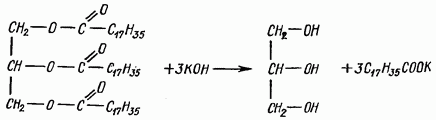
Реактивы: а) растительное масло или животный жир; б) кали едкое, 30%-ный спиртовой раствор; в) дистиллированная вода.
В широкую пробирку вносят 0,5 мл растительного масла или около 0,5 г животного жира и добавляют 10 мл спиртового раствора едкого кали. Пробирку закрывают пробкой с воздушным холодильником и нагревают на кипящей водяной бане в течение 30 мин., после чего в пробирку наливают горячую воду и растворяют в ней мыло.
Выделение свободных жирных кислот. Реактивы: а) раствор мыла (см. предыдущую работу); б) соляная кислота (1:1 по объему).
К 5 мл раствора мыла добавляют 1-2 мл раствора соляной кислоты. При взаимодействии сильной кислоты с мылом выделяются свободные жирные кислоты, которые всплывают на поверхность жидкости. Реакция идет по следующему уравнению:
Образование нерастворимых мыл. Кальциевые и магниевые соли жирных кислот нерастворимы в воде.
Реактивы: а) раствор мыла (см. работу «Омыление жира»); б) хлористый кальций, 5-10%-ный раствор.
К 2-3 мл раствора калийного мыла добавляют 1 мл раствора хлористого кальция. Выпадает нерастворимый в воде осадок стеарата кальция
Проба на непредельные жирные кислоты. Непредельные жирные кислоты способны присоединять галоиды по месту двойных связей:

Реактивы: а) растительное масло; б) бромная вода (хранят под тягой!); в) диэтиловый эфир или хлороформ.
В пробирку наливают 1-2 мл масла, растворяют его в 2-3 мл диэтилового эфира или хлороформа, прибавляют 1-2 капли бромной воды и взбалтывают. Буроватожелтая окраска бромной воды исчезает, что указывает на присутствие непредельных кислот.
Количественное определение жира. В основу многочисленных методов определения содержания жира в биологическом материале положена способность липидов растворяться в органических растворителях (диэтиловом и петролейном эфире, четыреххлористом
углероде, дихлорэтане, хлороформе и др.). При экстрагировании органическими растворителями в раствор переходят не только жиры, но также свободные жирные кислоты, фосфолипиды, стерины, воска, эфирные масла, пигменты (например, хлорофилл) и ряд других веществ, поэтому продукт, получаемый в результате анализа, называют «сырым жиром» или «суммой липидов». Для практических целей этот показатель обычно является достаточным, в случае же необходимости более точного определения «истинного жира» приходится в отдельных пробах материала исследовать содержание фосфолипидов (по фосфору), эфирных масел (перегонкой с водяным паром), свободных жирнкх кислот (тит-риметрическим методом) и т. д. и вносить соответствующие поправки в результаты анализа.
Приводим метод определения «сырого жира» в семенах масличных культур (по С. В. Рушковскому), нашедший широкое применение в лабораторной практике.
Реактивы и материалы; а) диэтиловый эфир. Для экстракции жира употребляют безводный эфир. В склянку с продажным эфиром прибавляют прокаленный хлористый кальций или негашеную известь (окись кальция). Сосуд укупоривают корковой пробкой, в которую вставляют трубку с прокаленным хлористым кальцием. По истечении 1-2 суток эфир сливают и к нему прибавляют новую порцию негашеной извести или хлористого кальция. Через 6-8 ч эфир сливают в сосуд, на дно которого кладут кусочки металлического натрия. Эфир должен быть также свободным от перекисей. Для этого к 1 л эфира добавляют раствора марганцовокислого калия и 10 мл 40%-ного раствора едкого кали или едкого натра, смесь осторожно взбалтывают и ставят в темное место на 20-24 ч, после чего разделяют в делительной воронке. Нижний слой, водный, отделяют, а верхний, эфирный, несколько раз промывают дистиллированной водой и затем обезвоживают, как описано выше. Внимание! Диэтиловый эфир легко воспламеняется, его пары образуют с воздухом взрывоопасные смеси, поэтому все работы надо проводить при строжайшем соблюдении противопожарных мероприятий. Целесообразно заменять диэтиловый эфир невоспламеняющимся растворителем, например четыреххлористым углеродом или хлороформом;
б) фосфорнокислый натрий двузамещенный, безводный, или сернокислый натрий, безводный. Кристаллическую соль высушивают в течение 6-8 ч при 100-105° С. Сернокислый натрий прокаливают в муфельной печи в течение семена льна, конопли, подсолнуха, рапса, кунжута.
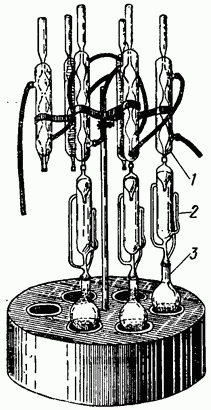
Рис. 11. Экстракционный аппарат Сокслета.
Аппаратура: а) экстракционный аппарат Сокслета (рис. 11). Состоит из трех частей, пришлифованных друг к другу: холодильника шарикового или спирального 1, экстрактора 2 и приемной колбы 3.
Берут 2-3 навески семян но 2-5 г (в зависимости от предполагаемого содержания масла). Навеску переносят в сухую фарфоровую ступку и растирают с безводным сернокислым натрием или фосфорнокислым натрием двузамещенным до получения однородной порошковидной массы. Соли берут в три раза больше по отношению к навеске.
Тщательно растертую массу количественно переносят в пакетик из фильтровальной бумаги, высушенной до постоянного веса. Пакетик заворачивают, как порошок в аптеке, взвешивают на аналитических весах и переносят в экстрактор аппарата Сокслета.
Примечание. В экстрактор можно поместить 4-6 пакетиков.
В приемную колбу наливают эфир (или другой растворитель) на емкости, после чего ее соединяют с экстрактором. В экстрактор наливают столько эфира, чтобы его уровень покрывал пакетики и почти доходил до верхней части сифона, затем с помощью шлифа соединяют его с холодильником и аппарат ставят на холодную водяную баню. Материал настаивают в растворителе
не менее 3-4 ч и лишь после этого включают источник нагрева.
Примечание. Аппараты Сокслета следует установить в вытяжном шкафу. Еще раз подчеркиваем необходимость тщательного соблюдения всех противопожарных мероприятий. Во время заливки эфира выключают все электроприборы в лаборатории.
Пары эфира из приемной колбы по широкой трубке поступают в холодильник, где они конденсируются, и капли растворителя стекают в экстрактор, извлекая жир из растертых семян. Как только уровень эфира достигнет верхнего края сифонной трубки, он тотчас же начнет переливаться в приемную колбу. Таким образом, процесс экстракции продолжается непрерывно. Диэтиловый эфир кипит при температуре 34-35° С, поэтому надо так отрегулировать нагрев, чтобы в течение часа происходило не более 8-10 сливаний растворителя через сифонную трубку.
Экстракцию жира продолжают 5-6 ч (не считая времени настаивания), после чего пакетики с обезжиренным материалом вынимают из экстрактора, подсушивают на стекле в вытяжном шкафу (до испарения эфира) и высушивают (во взвешенных бюксах) при 100-105° С до постоянного веса. Содержание масла в семенах (в процентах на сухое вещество) рассчитывают, зная вес пакетика до и после экстракции, а также вес пустого пакетика. Берут среднее из 3-4 определений.
Определение химических показателей жиров.
По своему составу природные жиры весьма неоднородны. Они состоят из смеси триглицеридов различных предельных и непредельных жирных кислот. Кроме того, в их состав входят также моно- и диглицериды, свободные жирные кислоты, пигменты, жирорастворимые витамины, некоторая примесь белковых веществ. Нейтральным жирам обычно сопутствуют липоиды (фосфатиды, стерины, стериды и т. д.).
Растительные жиры (называемые обычно маслами) характеризуются жидкой консистенцией. В их состав входят главным образом непредельные кислоты. Масло какао и кокосовое - твердые.
Жиры животного происхождения - преимущественно твердые, так как состоят в основном из глицеридов предельных жирных кислот. Животные жиры жидкой консистенции
Жиры характеризуются рядом химических показателей. Основные из них: кислотное число, число омыления, эфирное число, йодное число.
Примечание. Для более подробной характеристики химических свойств жнров определяют также содержание летучих кислот (растворимых и нерастворимых в воде), окснкислот (ацетильное число), родановое и гексабромное числа и некоторые другие показатели, рассмотрение которых не входит в задачи нашего практикума.
При хранении жира под влиянием кислорода воздуха, влаги и солнечного света, при участии органических катализаторов-ферментов происходит его порча, прогоркание. Растительные масла, богатые непредельными кислотами, прогоркают быстрее, чем твердые жиры. Степень устойчивости жиров при хранении характеризуют перекисное число и содержание альдегидов. В значительной мере об этом свидетельствует и кислотное число, так как при порче происходит гидролитический распад триглицеридов и высвобождение свободных жирных кислот.
Кислотное число. Кислотным числом называется количество миллиграммов едкого кали, необходимое для нейтрализации свободных жирных кислот, содержащихся в 1 г жира.
Реактивы: а) едкое кали, 0,1 н спиртовой раствор;
б) смесь этилового спирта с диэтиловым эфиром (1:1);
в) фенолфталеин, 1%-ный спиртовой раствор; г) тимол-фталеин, 1%-ный спиртовой раствор.
В сухую коническую колбу (емкостью 250 мл) отвешивают 3-5 г жира. Навеску растворяют в 50 мл предварительно нейтрализованной смеси спирта с эфиром.
Примечание. Смесь спирта с эфиром нейтрализуют 0,1 н спиртовым раствором едкого калн (в присутствии 3-4 капель раствора фенолфталеина) до слаборозового окрашивания и лишь после этого вливают в колбу с навеской жнра.
Раствор жира титруют 0,1 н спиртовым раствором едкого кали (индикатор - фенолфталеин) до появления розовой окраски, не исчезающей в течение 0,5-1 мин.
При определении кислотного числа темноокрашенных жиров вместо фенолфталеина пользуются 1%-ным спиртовым
раствором тимолфталеина (в кислой среде - бесцветен, в щелочной - голубое окрашивание).
Кислотное число к. ч. вычисляют по формуле
![]()
где в - количество 0,1 н спиртового раствора едкого кали, израсходованное на титрование навески жира, мл; к - поправочный коэффициент к титру 0,1 н раствора КОН; 5,611 - титр точно 0,1 н раствора КОН; н - навеска жира, г.
Для характеристики кислотности растительных масел, кроме кислотного числа, часто рассчитывают процентное содержание свободной олеиновой кислоты О по формуле
![]()
где к. ч. - кислотное число масла, мг.
Число омыления. Число омыления показывает, сколько миллиграммов едкого кали надо израсходовать для нейтрализации как свободных, так и связанных (в эфиры) кислот, содержащихся в 1 г жира.
Реактивы: а) растительное масло или животный жир; б) едкое кали, 0,5 н спиртовой раствор: 29-30 г гранулированного едкого кали растворяют в 25-30 мл воды, после чего для осаждения карбонатов прибавляют несколько миллилитров 35-40%-ного раствора хлористого бария и раствор в литровой мерной колбе доводят этиловым спиртом - ректификатом до метки. Хранят в хорошо укупоренной склянке оранжевого стекла. Для защиты от проникновения углекислоты воздуха склянку снабжают хлоркальциевой трубкой с натронной известью; в) соляная кислота, 0,5 н раствор; г) фенолфталеин, спиртовой раствор.
Коническую колбу (емкостью 250 мл) взвешивают на аналитических весах, затем в нее вносят около 2 г растительного масла или животного жира и снова взвешивают. По разности устанавливают навеску жира. В колбу с помощью пипетки с резиновой грушей вливают 25 мл 0,5 н спиртового раствора КОН, укупоривают пробкой с обратным холодильником и нагревают на водяной бане 35-40 мин., время от времени взбалтывая содержимое колбы. При омылении жира не следует допускать бурного
кипения воды в бане, которое может явиться причиной вспенивания жидкости в колбе и попадания ее на пробку. К концу процесса омыления раствор в колбе становится однородным, прозрачным, без капелек жира.
Горячий мыльный раствор в колбе оттитровывают 0,5 н соляной кислотой (индикатор - фенолфталеин) до обесцвечивания розовой окраски. Параллельно проводят контрольный опыт с тем же количеством 0,5 н спиртового раствора КОН, но без добавления жира. Контрольный опыт необходим для проверки титра раствора КОН, так как вследствие частичного проникновения углекислоты воздуха и окисления этилового спирта титр может меняться.
Число омыления о. рассчитывают по формуле
![]()
где с - количество 0,5 н раствора соляной кислоты, израсходованное на титрование контрольного («слепого») опыта, мл; - количество 0,5 н раствора соляной кислоты, израсходованное на титрование испытуемого образца, к - поправочный коэффициент к титру приблизительно 0,5 н спиртового раствора КОН; 28,055 - титр точного 0,5 н раствора КОН (1 мл раствора содержит 28,055 мг КОН); н - навеска жира, г.
Эфирное число. Эфирным числом называют количество миллиграммов едкого кали, которое требуется для нейтрализации жирных кислот, связанных в виде эфиров в 1 г жира.
Эфирное число э. ч. определяют расчетным путем, вычитая кислотное число из числа омыления:
Таким образом, число омыления является суммой кислотного и эфирного чисел.
Определение количества глицерина в жире.
Химическое определение содержания глицерина в жирах является довольно трудоемким и продолжительным. Сравнительно неплохие результаты дает расчетный метод. Зная эфирное число жира, можно вычислить содержание глицерина, приняв во внимание, что для высвобождения одной молекулы глицерина надо израсходовать три молекулы едкого кали
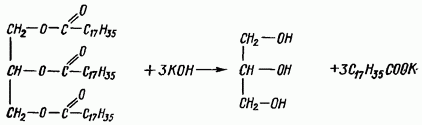
Процентное содержание глицерина в жире г рассчитывают по формуле
![]()
где 92,06 - молекулярный вес глицерина; э. ч. - эфирное число жира; 56,11 - молекулярный вес едкого кали.
Иодное число.
Общие сведения. Иодное число показывает количество граммов иода, которое присоединяется к 100 г жира. Оно свидетельствует о количественном содержании непредельных кислот в жире, что позволяет судить о его устойчивости к окислению, полимеризации и другим превращениям. Йодное число является показателем, характерным для каждого вида свежего жира.
Химизм процесса присоединения галоидов описан выше (см. «Проба на непредельные жирные кислоты»). Следует подчеркнуть, что иод присоединяется главным образом к двойным связям, тогда как более реакционноспособные галоиды - хлор и бром - могут также замещать атомы водорода в углеводородном радикале кислоты.
Наиболее точным является определение йодного числа то Гюблю, однако оно связано с применением весьма ядовитого реактива - сулемы и поэтому не может быть рекомендовано для студенческого практикума. Описываем более простой и быстрый метод определения йодного числа, применение которого не связано с использованием сулемы. Метод обладает вполне удовлетворительной точностью.
Определение йодного числа с бромистым иодом (по Ганусу). Бромистый иод образуется при взаимодействии иода с бромом в уксуснокислой среде.
Бромистый иод количественно присоединяется к непредельным жирным кислотам по месту двойных связей.
Избыток бромистого иола, не вошедший в реакцию, реагирует с иодистым калием по уравнению
Выделившийся иод оттитровывают тиосульфатом
Реактивы: а) растительное масло; б) реактив Гануса: 13 г кристаллического иода растворяют в 100 мл ледяной уксусной кислоты (в мерной колбе емкостью . К раствору добавляют 8,2 г брома и доводят ледяной уксусной кислотой до 1 л. Хранят в склянке оранжевого стекла с притертой пробкой. Раствор готовится лаборантом (в вытяжном шкафу!); в) иодистый калий, 20%-ный раствор. Готовится непосредственно перед определением; г) тиосульфат натрия (гипосульфит, серноватистокислый натрий), 0,1 н раствор; д) крахмал, 1%-ный раствор; е) хлороформ.
В сухую коническую колбу или склянку с притертой пробкой емкостью 250-300 мл отвешивают на аналитических весах 0,2-0,3 г масла и растворяют его в 10 мл хлороформа. В другую такую же колбу или склянку вносят 10 мл хлороформа без масла («слепой опыт»), В обе колбы из бюретки (со стеклянным краном) добавляют по 25 мл реактива Гануса. Сосуды плотно закрывают пробками, смоченными в растворе иодистого калия. Содержимое сосудов осторожно взбалтывают, после чего сосуды ставят в темное место на 1-1,5 ч. По истечении указанного времени в оба сосуда добавляют по 10 мл 20%-ного раствора иодистого калия и 50 мл воды и выделившийся иод оттитровывают 0,1 н раствором тиосульфата натрия до слабо-желтой окраски, потом добавляют 10-12 капель раствора крахмала и продолжают титрование до полного обесцвечивания раствора.
При расчетах принимают во внимание, что 1 мл 0,1 н раствора тиосульфата натрия соответствует 1 мл 0,1 н раствора иода. Йодное число и. ч. вычисляют по формуле
где с - количество 0,1 н раствора тиосульфата, израсходованное на титрование контрольной пробы («слепой опыт»), - количество 0,1 н раствора тиосульфата,
израсходованное при титровании опытного образца, к - поправочный коэффициент к титру приблизительно 0,1 н раствора тиосульфата; 0,01269 - титр раствора тиосульфата по иоду; н - навеска масла, г.
Перекисное число.
Общие сведения. Непредельные жирные кислоты легко подвержены окислению. Этот процесс протекает под воздействием кислорода воздуха, влаги, света и катализируется ферментом липоксигеназой (липооксидазой).
Перекиси - неустойчивые соединения. Они легко распадаются с образованием окисей и освобождением атомарного кислорода. Атомарный кислород в свою очередь служит источником образования озона и перекиси водорода.
В дальнейшем перекиси и окиси превращаются в оксикислоты.
Выделившийся озон окисляет новые молекулы непредельных кислот. Образуются нестойкие соединения, озониды, которые гидролитически расщепляются, превращаясь в альдегиды.
Вот почему определение содержания перекисей и альдегидов может оказать большую помощь при суждении о качестве растительного масла.
Определение перекисного числа. Количественное определение перекисей в растительном масле основано на реакции выделения иода перекисями из иодистого калия в кислой среде
Иод оттитровывают раствором тиосульфата.
Реактивы: а) растительное масло (лучше прогорклое); б) уксусная кислота, ледяная; в) хлороформ, химический чистый (лучше - для наркоза); г) калий иодистый, насыщенный раствор. Готовится перед употреблением; д) тиосульфат натрия (гипосульфит, серноватистокислый натрий), 0,002 н раствор. Готовят перед употреблением из 0,1 н раствора: в мерную колбу на 250 мл с помощью пипетки вносят 5 мл 0,1 н раствора и
доводят до метки прокипяченной (и затем охлажденной до 20° С) дистиллированной водой; е) крахмал, 0,5%-ный раствор.
В конической колбе или склянке с притертой пробкой емкостью 200 мл отвешивают (на аналитических весах) около 2 г масла. Навеску растворяют в 20 мл смеси ледяной уксусной кислоты и хлороформа (2:1 по объему), прибавляют 5 мл насыщенного раствора иодистого калия, сосуд укупоривают пробкой и ставят в темное место на 10 мин., после чего доливают 50 мл дистиллированной воды и оттитровывают выделившийся иод 0,002 н раствором тиосульфата (индикатор - крахмал). Одновременно проводят также контрольное определение (без масла).
Перекисное число п. ч. (количество граммов иода, выделенное перекисями, содержащимися в 100 г масла) рассчитывают по формуле
где с - количество 0,002 н раствора тиосульфата, израсходованное при контрольном определении, - количество 0,002 н раствора тиосульфата, израсходованное при титровании опытного образца, мл; k - поправочный коэффициент раствора тиосульфата; 0,0002538 - титр 0,002 н раствора тиосульфата по иоду (1 мл раствора соответствует 0,0002538 г иода); н - навеска масла, г.
Качественная реакция на альдегиды (с реактивом Шиффа).
Одной из наиболее специфичных является реакция альдегидов с фуксинсернистой кислотой (реактивом Шиффа). Бесцветный раствор фуксинсернистой кислоты под влиянием альдегидов принимает красно-фиолетовое или сине-фиолетовое окрашивание.
Реакция протекает по следующей схеме:
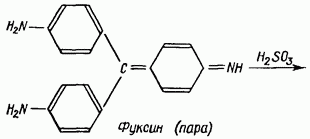
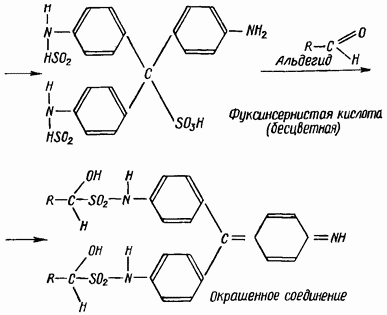
Реактивы. Реактив Шиффа; можно готовить двумя способами: а) 0,5 г фуксина растворяют в 500 мл воды и фильтруют. 500 мл воды насыщают сернистым ангидридом. Оба раствора сливают вместе и оставляют на 10-12 ч. Хранят в темном месте; б) в мерную колбу емкостью 250 мл вливают 30 мл 0,1%-ного спиртового раствора фуксина, добавляют 15 мл 32%-ного водного раствора сернистокислого натрия воды. Содержимое колбы осторожно перемешивают и оставляют на 1 ч, после чего прибавляют 16 мл разведенной серной кислоты (1:3) и доливают до метки 50%-ным этиловым спиртом. Хранят в склянке темного стекла или темном месте. При исследовании масел предпочтительнее пользоваться реактивом, приготовленным по второму способу.
В пробирку наливают 5-6 мл масла, добавляют 2-3 мл реактива Шиффа и взбалтывают. В случае наличия альдегидов жидкость окрасится в сине-фиолетовый или красно-фиолетовый цвет. Максимум окрашивания развивается через 15-16 мин. Если окраска не появляется через 20 мин. после начала опыта, то это свидетельствует об отсутствии альдегидов в масле.
Разделение и идентификация высших предельных жирных кислот с помощью хроматографии на бумаге.
Общие сведения. С помощью описываемого метода
можно разделить и идентифицировать высшие предельные (насыщенные) жирные кислоты, в состав которых входит от 12 до 24 атомов углерода.
Общая методика разделения органических веществ на бумаге описана выше (см. «Распределительная хроматография аминокислот на бумаге»).
Для хроматографирования жирных кислот применяют специально подготовленную гидрофобную бумагу. Высшие жирные кислоты являются гидрофобными веществами, поэтому при хроматографировании исключается применение воды в качестве неподвижной фазы. Роль подвижной фазы обычно выполняет ледяная уксусная кислота или смесь уксусной кислоты с муравьиной и водой (30: 10: 1).
Метчики: пальмитиновая, стеариновая и другие высшие предельные жирные кислоты.
Подготовка хроматографической бумаги. Бумагу промывают 0,5%-ным раствором соляной кислоты в течение 3 мин., после чего 5-6 раз дистиллированной водой, 3 раза этиловым спиртом и 4-5 раз диэтиловым эфиром, затем высушивают на воздухе (работу проводят под тягой, при выключенных нагревательных приборах, соблюдая при этом противопожарные мероприятия).
Промытую и высушенную бумагу разрезают на полоски шириной 1-2 см и длиной 30-35 см. Один край каждой полоски прокалывают иголкой с ниткой, образуя петлю. Для гидрофобизации полоски опускают в цилиндр с притертой пробкой, на дно которого (слоем высотой в 4-6 см) налит бензольный раствор вазелинового масла. Нитяные петли подводят под пробку и сосуд плотно укупоривают. Полоски вынимают, когда раствор дойдет до верхнего края бумаги (на 1 см до петли), и высушивают при комнатной температуре (в вытяжном шкафу). При обработке керосином полоски погружают в жидкость на 1 мин., потом вынимают, отжимают роликом между двумя листами фильтровальной бумаги и высушивают в висячем положении при комнатной температуре (в вытяжном шкафу).
Выделение смеси жирных кислот. В коническую колбу вносят 2-3 г жира и добавляют 20- 25 мл 25%-ного спиртового раствора едкого кали. Колбу плотно закрывают пробкой с обратным холодильником, ставят на кипящую водяную баню и проводят омыление жира в течение 35-40 мин. К раствору мыла в колбе прибавляют 25-30 мл горячей воды и перемешивают. Раствор переливают в выпарительную чашку и нагревают на горячей водяной бане (температура воды не выше 85° С) до полного исчезновения запаха спирта. К жидкости в чашке добавляют несколько миллилитров раствора серной кислоты (1:3) до полного выделения слоя жирных кислот. Содержимое чашки осторожно переливают в делительную воронку. Отделяют водно-кислотный слой, а слой жирных кислот несколько раз промывают теплой водой до нейтральной реакции промывных вод по метилоранжу. Промытый слой жирных кислот фильтруют через сухую фильтровальную бумагу в темную склянку с притертой пробкой и хранят в холодильнике.
Для хроматографирования готовят раствор жирных кислот в толуоле или ацетоне, или метиловом спирте, или смеси этилового спирта с диэтиловым эфиром. Отдельно готовят раствор метчиков (в том же растворителе). Концентрацию кислот в растворах подбирают так, чтобы в капле, нанесенной микропипеткой на бумагу, содержалось 10-25 мкг каждой кислоты.
Хроматографирование. На расстоянии 1-1,5 см от нижнего края бумажной полоски графитовым
карандашом вычерчивают прямую линию, на которую с помощью микропипетки наносят каплю испытуемого раствора. На другую такую же полоску наносят каплю раствора метчиков. Капли высушивают на воздухе.
Разделение производят в стеклянных цилиндрах с притертыми пробками при комнатной температуре. На дно цилиндра наливают ледяную уксусную кислоту или смесь уксусной кислоты, муравьиной кислоты и воды . Полоску подвешивают за нитяную петлю, которую подводят под пробку так, чтобы нижний край бумаги был погружен в жидкость на 3-5 мм.
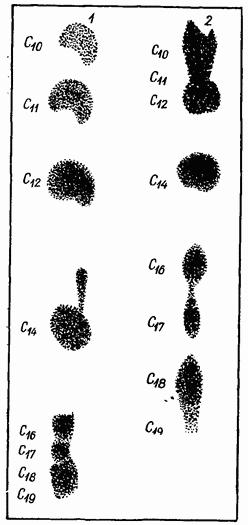
Рис. 12. Хроматограмма жирных кислот.
После того как растворитель поднялся по бумаге на 26-28 см, полоски вынимают и высушивают при комнатной температуре, затем промывают в дистиллированной воде и снова высушивают.
В фотографическую ванночку наливают раствор основного азотнокислого висмута, в который кладут хроматограммы на 10-15 мин., затем их перекладывают в другую ванночку с дистиллированной водой, которую меняют 10-12 раз. Хорошо промытые полоски опрыскивают раствором сульфгидрата аммония (или кладут в ванночку с раствором): появляются черные пятна жирных кислот (рис. 12). Хроматограммы 5-6 раз промывают дистиллированной водой и высушивают на воздухе. Рассчитывают каждой кислоты
на опытной и контрольной хроматограммах (с метчиками) и по совпадению их мест устанавливают состав кислот испытуемого жира.
